آلکاپتونوری یک نوع اختلال نادر ژنتیک است که با تجمع هموژنیستیک اسید در بدن مشخص میشود. افراد مبتلا به این اختلال دچار کمبود آنزیم هموژنتیستیک دی اکسی ژناز (HGD) هستند. این آنزیم ماده سمی هموژنتیستیک اسید را تجزیه میکند. در این شرایط، ادرار در معرض هوا به رنگ سیاه درمیآید.
آلکاپتونوری چیست؟
آلکاپتونوری (AKU) بوسیله نقص هموژنتیسات ۱و۲- دی اکسی ژناز مشخص میشود که هموژنتیستیک اسید (HGA) را به مالیلاکتواستئیک اسید (maleylacetoacetic) در مسیر تخریب تیروزین، ایجاد میشود. سه ویژگی عمده آلکاپتونوریا با وجود HGA در ادرار، اونکروز (رنگدانههای سیاه و سفید مایل به آبی در بافت پیوندی)، آرتروز ستون فقرات و مفاصل بزرگتر است. اکسیداسیون HGA منتشر شده در ادرار، فراوردهای شبه ملانین تولید میکند و موجب تیره شدن حالت ادرار میشود. رنگدانه آبی سیاه، تنها پس از ۳۰ سالگی ظاهر میشود؛ آرتروز نیز در دهه سوم زندگی شروع میشود. سایر ویژگیهای این بیماری شامل رسوب رنگدانه، مشکلات قلبی عروقی، سنگ کلیه و سنگ پروستات است.
علائم
افرادی که دچار این بیماری هستند تا زمان بزرگسالی از این بیماری آگاه نیستند. علائم معمولا به کندی پیشرفت میکنند. ادرار افراد مبتلا، به صورت غی طبیعی تیره است یا ممکن است در معرض هوا تیره شود. البته از آن جایی که این تغییر ممکن است چند ساعت به طول بینجامد، اغلب مورد توجه قرار نمیگیرد. به هنگام نوزادی، پوشک بچه ممکن است حاوی رنگدانه سیاه شود که اغلب اوقات نادیده گرفته میشود.
نخستین علامت مشخص آلکاپتونوری معمولا تا ۳۰ سالگی مشخص نمیشود و به دلیل تجمع هموژنتیستیک اسید در بافت پیوندی به خصوص غضروف است. در بسیاری افراد ممکن است غضروف داخل گوش، ضخیم، نامنظم و ابی رنگ یا خاکستری یا سیاه شود. نهایتا این تغییر رنگ ممکن است روی پوست پوشش دهنده غضروف هم ظاهر شود. در بسیاری موارد، سفیدی چشم نیز تغییر رنگ پیدا میکند. البته این رنگدانه در بینایی اختلال ایجاد نمیکند. علائم آن به طور خلاصه به صورت زیر هستند:
- لکههای سیاه در بخش سفید چشم
- ضخیم، بی نظم و تیره شدن غضروف داخل گوشها
- آرتروز مفصلی در ستون مهرهها و مفاصل بزرگ (بخصوص لگن، زانو و شانه)
- سنگ کلیه و سنگ پروستات
- اختلالات دریچههای قلب و عروق قلبی
- لکههای آبی روی پوست به خصوص در اطراف غدد عرق
- سیاه شدن موم گوش
تجمع هموژنتیستیک اسید موجب سفت شدن دریچههای قلب میشود. این کار از بسته شدن آنها به طور صحیح، جلوگیری میکند که منجر به اختلالات دریچه میترال و آئورت میشود. در موارد شدید، دریچه میترال تعویض میشود. سخت شدن عروق منجر به فشار خون بالا میشود.
علل
جهش در ژن هموژنیستات ۱و۲ دی اکسی ژناز (HGD) موجب آلکاپتونوری میشود. این بیماری به صورت اتوزومی منتقل میشود. به این معنی که هر دو والدین باید این ژن را داشته باشند تا این بیماری بوجود آید. میزان شیوع دقیق آلکاپتونوریا نامشخص است اما معمولا از ۲۵۰ هزار تا ۱ میلیون تولد، تها ۱ نفر داراری این بیماری است. این بیماری در تمام قومیتها گزارش شده است. مناطقی در اسلواکی، جمهوری دومینیکن و آلمان با افزایش فراوانی این اختلال شناسایی شدهاند.
تشخیص
پزشکان معمولا با معاینه بیمار و نگاه کردن به ظاهر وی متوجه برخی علائم میشوند. در صورتی که فرد دچار آلکاپتونوری پیشرفته باشد، لکههای تیره در قسمت سفیدی چشم، لکههای آبی رو به سیاه روی غضروف و همچنین روی پوست، مشهود است. همچنین در صورتی که ادرار در معرض هوا به رنگ قهوهای یا سیاه دربیاید، به این بیماری مشکوک میشود. اگر کسی دچار استئوآرتریت باشد، آن را نیز تست خواهد کرد.
پزشک از تست کروماتوگرافی گاز برای دیدن رگههای هموژنتیستیک در ادرار استفاده میکند. همچنین تست ژنتیک هم برای بررسی ژن جهش یافته HGD، استفاده خواهد کرد. برای تشخیص آلکاپتونوری، گرفتن سابقه خانوادگی شخص مفید است. البته بسیاری از افراد از داشتن چنین ژنی آگاه نیستند. والدین هم ممکن است ناقل باشند بدون آنکه از داشتن این ژن آگاه باشند.
در افراد بالای ۴۰ سال، نوار قلب هم توصیه میشود تا اختلالات قلبی احتمالی همچون اتساع آئورت یا سختی یا نارسایی آئورت یا دریچههای میترال بررسی شود. اکوی قلب، امواج مافوق صوت را به قلب فرستاده و انعکاس آنها را که از قلب خارج میشود، روی مونیتور مشاهده میکند تا عملکرد و حرکت قلب را مطالعه کند. برای تشخیص سختی عروق کرونر، عمدتا سی تی اسکن قلب توصیه میشود. در این صورت تصاویر با جزئیات بیشتر به پزشک تحویل داده میشود.
درمان آلکاپتونوری
هیچ درمان خاصی برای آلکاپتونوری وجود ندارد و درمان بیشتر برای رفع علائمی ست که در بیمار ظاهر میشود. برای افراد مبتلا به این بیماری داروهای ضد التهاب داده میشود تا درد مفصلی درمان شود. در موارد شدید، داروهای قویتری همچون داروهای ضد درد تخدیری، توصیه میشود. کنترل درد متناسب با وضعیت خاص هر فرد است و نیاز به پیگیری طولانی مدت و تطبیق با فرد دارد.
انجام جلسات فیزیوتراپی و کار درمانی که به کشش و انعطاف پذیری عضلات و مفاصل کمک میکند، برای برخی افراد مفید است. مشاوره ژنتیک هم برای افراد مبتلا و خانوادههای انها خوب است.
برخی افراد مبتلا به آلکاپتونوری نیاز به مداخله جراحی ارند. تقریبا نیمی از افراد مبتلا به این بیماری در سنین ۵۰ تا ۶۰ سال، نیاز به جایگزینی مفصل، لگن، زانو یا شانه دارند. این افراد به ندرت، نیاز به جراحی ستون فقرات، ازجمله جوش خوردن یا برداشتن دیسکهای کمر دارند. جراحی برای تعویض دریچههای آئورت یا میترال نیز ممکن است لازم باشد. در بعضی موارد، سنگهای کلیه یا پروستات هم باید با جراحی یا درمان پیشگیرانه از بین بروند.
ثابت شده که محدودیتهای رژیم غذایی به کل بی اثر هستند. مصرف پروتئین لازم است و ثابت شده که حفظ آن به به مدت طولانی برای این افراد، دشوار است. علاوه بر این محدودیت شدید و طولانی مدت در مصرف پروتئین میتواند عوارضی را به همراه داشته باشد.
در کودکان و بزرگسالان هم دوزهای بالای ویتامین C برای درمان آلکاپتونوری موثر است؛ زیر ا از تجمع و رسوب اسید هموژنتیستیک ممانعت میکند. البته استفاده طولانی مدت از ویتامین C به صورت کلی اثبات نشده است و مطالعات قطعی بالینی در مورد اثر آن وجود ندارد.
باید از انجام فعالیتهایی که فشارهای جسمی قابل توجهی به ستون فقرات و مفاصل وارد میشود، مانند ورزشهای با ضریه زیاد یا کار شدید دستی خودداری شود.
درمانهای در حال تحقیق برای آلکاپتونوری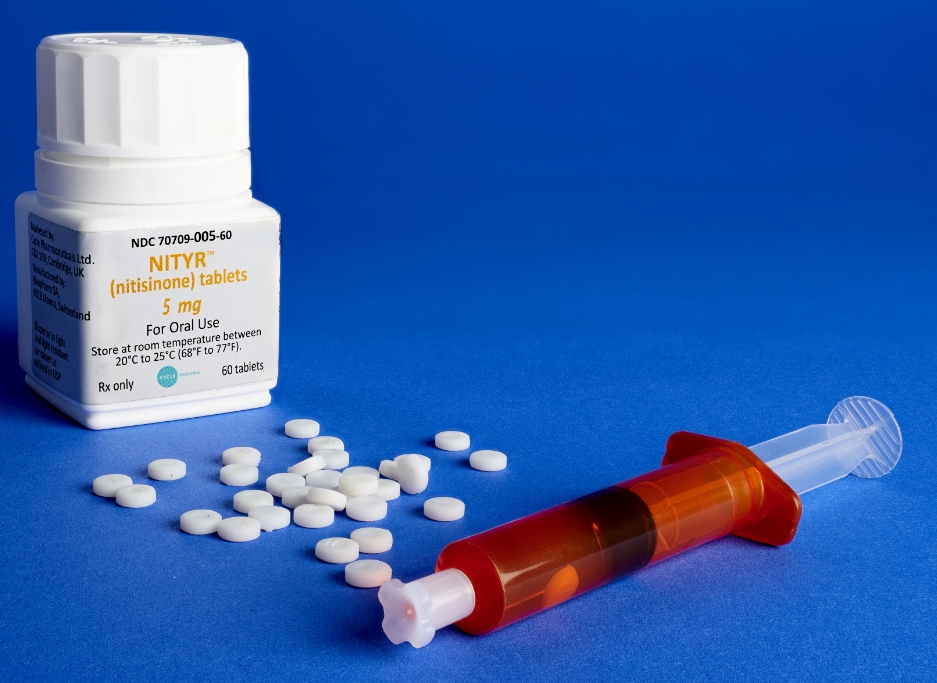
پژوهشگران در حال مطالعه در مورد استفاده از دارویی به نام نیتیزینون به عنوان درمان بالقوه آلکاپتونوریا هستند. این دارو در سال ۲۰۰۱، از طرف سازمان غذا و داروی آمریکا جزو داروهای کم کاربرد برای درمان اختلال متابولیک تیروزینمی پذیرفته شده است. در تحقیقات اولیه، نیتیزینون، کاهش چشمگیری در اسید هموژنتیستیک در افراد مبتلا به آلکاپتونوریا ایجاد کرد. البته باید تحقیقات بیشتری انجام شود تا استفاده از آن برای پیشگیری از علائم آلکاپتونوری برای افراد جوانتر و همچنین بی خطر بودن در استفاده طولانی مدت، مشخص شود.
چشم انداز بیماری در بلند مدت
امید به زندگی در افراد مبتلا به آلکاپتونوریا کاملا طبیعی است. با این وجود این بیماری، فرد را بیشتر در معرض اختلالات زیر قرار میدهد:
- آرتروز مهرهها، لگن، شانه و زانو
- پاره شدن تاندون آشیل
- سفت شدن دریچههای آئورت و میترال
- سفت شدن عروق کرونر
- سنگ کلیه و پروستات
بعضی از این اختلالات را میتوان با چکاپ منظم به تاخیر انداخت. پزشک از بیمار میخواهد تا به طور منظم بررسی شود. تستهای کنترل پیشرفت بیماری عبارتند از:
- عکس رادیولوژی از ستون مهرهها برای بررسی تخریب دیسک و سخت شدن مهرههای کمر
- عکس از قفسه سینه برای کنترل دریچههای آئورو میترال
- سی تی اسکن قلب برای یافتن علائم بیماری عروق کرونر
ترجمه و تالیف اختصاصی توسط مجله قرمز
منابع
ncbi




